炎症性肠炎是一组以消化系统持续性炎症为特征的慢性疾病,主要包括溃疡性结肠炎和克罗恩病[1]。溃疡性结肠炎的炎症主要位于结肠和直肠的黏膜和黏膜下层,患者发作期间常出现剧烈腹痛、持续腹泻,粪便多带鲜血,可夹杂黏液和脓性分泌物,长期病程还可能增加结肠癌发病风险[2,3]。
目前,溃疡性结肠炎在发达国家发病率较高,随着全球化进程加快和生活方式转变,其全球发病率逐步上升,尤其在亚洲地区更为明显[4,5]。由于对该病黏膜损伤机制及持续发病机制的理解仍有限,3%葡聚糖硫酸钠(DSS)诱导的小鼠结肠炎模型成为应用最广泛的实验模型,为溃疡性结肠炎的机制探索、药物研发及诊疗转化提供了高效可控的实验平台。
一、模型诱导原理
3%DSS诱导小鼠溃疡性结肠炎的核心机制为“三重作用恶性循环”:DSS对肠道黏膜的直接损伤、诱导机体产生异常免疫炎症反应、破坏肠道菌群稳态,三者相互作用,最终形成与人类溃疡性结肠炎病理特征高度相似的病变状态。
二、模型诱导后的主要变化
2.1 临床表现改变
造模第3天左右,小鼠开始出现粪便隐血阳性或肉眼可见血便;第4~7天症状逐渐加重,表现为明显黏液血便、腹泻,部分小鼠出现肛周污秽。随着DSS饮用时间延长,小鼠活动量减少、精神萎靡,出现“缩背”姿势,毛发粗糙无光泽,严重时可出现死亡。
2.2 病理学改变
2.2.1 宏观形态改变
与空白对照组相比,模型组小鼠结肠长度显著缩短;肉眼可见结肠肠段充血、水肿,血管纹理模糊,肠壁质地变脆,严重时可见明显溃疡及出血点。
2.2.2 微观结构改变
模型组小鼠结肠黏膜上皮细胞广泛缺失,基底膜断裂,可见大片上皮组织脱落;隐窝结构变形、萎缩甚至完全破坏,杯状细胞数量显著减少;黏膜层及黏膜下层可见大量炎症细胞浸润,以中性粒细胞为主,同时可见巨噬细胞、淋巴细胞及浆细胞;部分区域可见多发性灶状溃疡及隐窝脓肿。
2.2.3 分子水平改变
DSS可直接损伤结肠上皮细胞,下调Occludin、ZO-1、Claudin-1等紧密连接蛋白表达,破坏肠道黏膜屏障完整性;促炎因子(TNF-α、IL-1β、IL-6等)大量分泌,抑炎因子(IL-10)表达下降,导致炎症失衡;大量巨噬细胞被募集至结肠病变部位并活化,分泌大量促炎细胞因子及趋化因子,进一步加剧黏膜损伤;同时,DSS可改变肠道微生态环境,降低菌群多样性及稳定性,引发菌群失调,进一步激活免疫炎症反应。
2.3 变化总结
3%DSS诱导的急性溃疡性结肠炎模型中,小鼠可出现典型腹泻、便血等临床表现,结肠肠段出现充血、水肿、溃疡及出血点,肠绒毛受损、隐窝结构变形,伴随肠道物理屏障破坏及异常免疫炎症反应,与人类溃疡性结肠炎病理特征高度契合。
三、实验材料与方法
3.1 实验材料
3.1.1 实验动物
选用6只6~8周龄C57BL/6J雄性小鼠,体重20~22 g;饲养环境控制为温度22~25℃、湿度55%~60%,12 h光照/12 h黑暗交替,实验前适应性饲养1周。
3.1.2 试剂与仪器
试剂:硫酸葡聚糖钠盐(麦克林,货号D808272)、生理盐水、异氟烷、通用型组织固定液(多聚甲醛);
仪器:15 mL离心管、常规手术器械(剪刀、镊子)、蠕动泵、超薄切片机、显微镜等。
3.1.3 药物配制
按硫酸葡聚糖钠盐粉末:生理盐水=3 g:100 mL的比例,称取适量硫酸葡聚糖钠盐粉末,溶解于生理盐水中,配制为3%DSS溶液,倒入小鼠饮用水壶中备用。
3.2 模型建立
3.2.1 实验分组
将适应性饲养7 d的C57BL/6J雄性小鼠随机分为2组,每组3只,具体分组如下:
• 空白对照组:正常自由饮水,连续7 d;
• 3%DSS模型组:自由饮用3%DSS溶液,连续7 d。
3.2.2 造模后取材与处理
(1)心脏灌注:采用手术剪逐层剪开小鼠胸前皮肤及皮下组织,暴露心脏;剪开右心耳,在左心室插入一次性静脉输液针,通过蠕动泵缓慢灌注生理盐水,直至肝脏颜色变白、心脏流出液呈透明色,且小鼠四肢末端及口唇发白,即完成灌注。
(2)结肠组织取材:用无菌手术剪取小鼠结肠组织,放入通用型组织固定液(多聚甲醛)中固定,经石蜡包埋后制作结肠病理切片,采用H&E染色法处理,通过显微镜观察结肠组织结构病理改变,用于模型成功与否的评价。
3.2.3 模型成功判定标准
肠黏膜层厚度变薄,黏膜上皮细胞破损,杯状细胞数量显著减少,炎症细胞浸润至黏膜下层,伴随少量充血,即为造模成功。
3.3 实验结果
3.3.1 小鼠临床表现结果
空白对照组小鼠排便正常,肛周干净无血迹,精神状态良好,毛发顺滑有光泽;3%DSS模型组小鼠毛发凌乱,精神萎靡,出现明显血便及肛周污秽,符合结肠炎典型临床表现。

图1 空白对照组与3%DSS模型组小鼠临床变化对比
3.3.2 小鼠结肠解剖形态结果
空白对照组小鼠结肠颜色正常、长度适中,肠壁质地柔软,血管纹理清晰;3%DSS模型组小鼠结肠呈暗红色(提示内部有血便),结肠长度显著缩短,肠壁充血水肿、质地变脆。

图2 造模7 d后空白对照组与3%DSS模型组小鼠结肠解剖形态对比
3.3.3 小鼠结肠组织病理学结果(H&E染色)
空白对照组小鼠结肠黏膜形态完好,黏膜层厚度正常,黏膜上皮细胞排列规则,可见大量杯状细胞,无炎症细胞浸润;3%DSS模型组小鼠结肠黏膜层厚度变薄,黏膜上皮细胞破损,杯状细胞数量显著减少,结肠隐窝结构破坏,伴有大量炎症细胞浸润,且炎症细胞浸润至肌层。
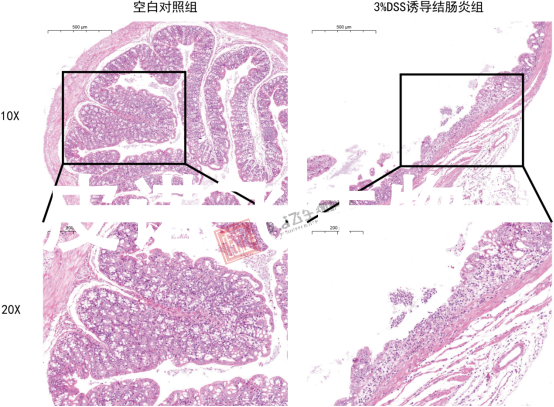
图3 造模7 d后空白对照组与3%DSS模型组小鼠结肠H&E染色结果(×200)
3.4 实验总结
本实验成功构建小鼠3%DSS诱导结肠炎模型。模型组小鼠表现出明显的血便、肛周污秽等临床表现;结肠解剖可见明显红肿、溃疡,结肠长度显著缩短;H&E染色结果显示结肠隐窝破坏、肠绒毛减少,大量炎症细胞浸润,完全符合模型成功判定标准,可用于后续溃疡性结肠炎相关实验研究。
四、参考文献
1. Ng S C , Shi H Y , Hamidi N ,et al.The Worldwide Incidence and Prevalence of Inflammatory Bowel Disease in the 21st Century: A Systematic Review of Population-Based Studies[C]//Digestive Disease Week.2017:S970-S971.
2. Hoivik M L , Moum B , Solberg I C ,et al.Work disability in inflammatory bowel disease patients 10 years after disease onset: results from the IBSEN Study[J].Gut, 2013, 62(3):368-375.
3. Mizoguchi A, Mizoguchi E. Inflammatory bowel disease, past, present and future: lessons from animal models. J Gastroenterol. 2008;43(1):1-17.
4. Molodecky N A ,Ing Shian Soon §, Rabi D M ,et al.Increasing Incidence and Prevalence of the Inflammatory Bowel Diseases With Time, Based on Systematic Review[J].Gastroenterology, 2012, 142( 1):46-54.
5. Jeong D Y , Kim S , Son M J ,et al.Induction and maintenance treatment of inflammatory bowel disease: A comprehensive review[J].Autoimmunity reviews, 2019, 18(5):439-454.