服务介绍:
肝癌是我国发病率和死亡率最高的四大癌症类疾病之一,然而肝癌的致病原因及其发病机制等迄今尚不完全清楚,肝癌临床治疗方面存在着患者初诊已为晚期、早期肝癌诊断难、术后复发转移率高、治疗缺乏针对性、源头创新药物和治疗手段少、预后较差以及肝癌患者年龄构成逐步年轻化等各种难题,新的抗肝癌药物研发意义重大。由于皮下肿瘤生物学特征导致皮下瘤往往形成纤维包膜结构,从而很难发生转移且缺乏免疫豁免区环境,从而模型的应用程度受限;而原位移植瘤模型具有肿瘤原发位点的典型特征,实验结果更接近临床。目前实验室采用C57小鼠肝膜下原位接种细胞方式构建小鼠肝原位瘤模型。
名称 | 规格 | 价格(元) |
裸鼠肝原位瘤 | 只 | 800起(方案询价) |
实验结果展示:
1、Hepa1-6肝原位瘤小鼠大体图

2、Hepa1-6肝原位瘤肝脏HE染色图
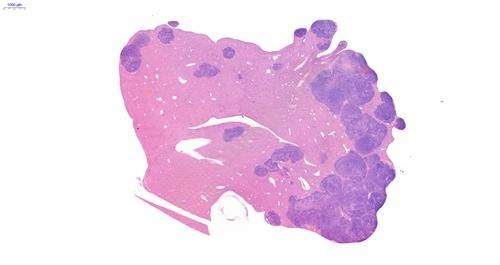
3、C57小鼠肝原位瘤大体图
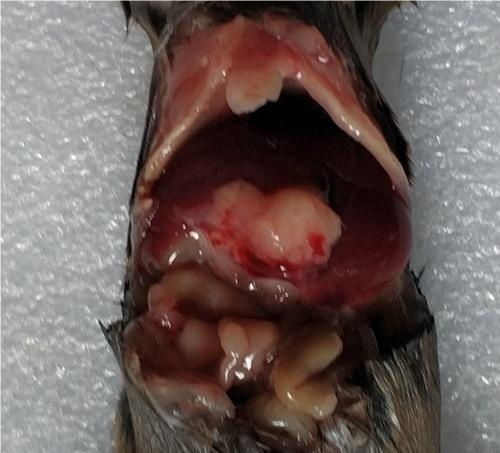
4、Hepa1-6-Luc肝原位瘤活体成像图
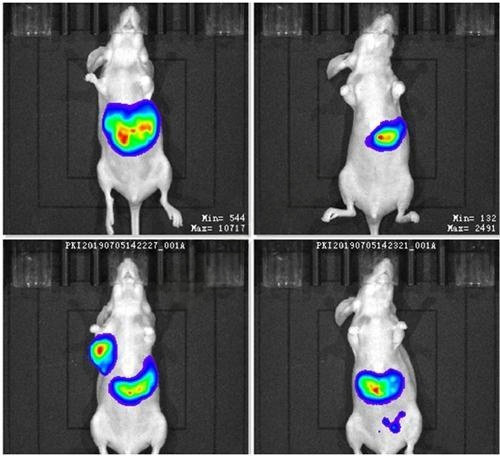
实验流程:
接收方案报价-预付款收取-细胞培养-动物订购-肝原位接种-成瘤指标监测-拍照取材-结果发送
送样运输要求:
冻存细胞需要直接寄到平台,尽量避免因温度转换导致细胞出问题
寄送细胞和药品时间:周天-周三,特殊情况需和平台沟通确定,避免出现因未及时收货导致样品出现问题
寄送细胞和样品需要附送送样单(备注清楚细胞名称,培养条件等)