Ti3C2Tx MXene纳米片被设计用于联合癌症治疗和抗炎药物递送系统。其独特的性质使其成为有效的药物载体,可在治疗过程中释放药物以实现精准、高效的治疗。此外,MXene纳米片还可以作为载体,帮助将药物递送至特定位置,实现针对性治疗。这种创新的药物递送系统不仅可以减少药物对健康细胞的损伤,还可以增强药物的生物利用率。Ti3C2Tx MXene纳米片的应用具有巨大的潜力,在癌症治疗和抗炎领域展现出无限可能。
近日,湖北武汉的科研工作者对Ti3C2Tx MXene纳米片有了新的研究成果。
《基于Ti3C2Tx MXene纳米片用于联合癌症治疗和抗炎的药物递送/级联酶系统》
文献链接https://www.sciencedirect.com/science/article/pii/S2352940724001616?via%3Dihub
参与此次科研单位:
a.教育部功能材料绿色制备与应用重点实验室;湖北大学材料科学与工程学院高分子材料湖北重点实验室;
b.湖北工业微生物重点实验室;国家“111”细胞调控与分子制药中心;湖北工业大学河滨分校格林;菲利普斯胶体研究中心;
c.湖北大学卫生科学与工程学院国家与地方高通量药物筛选技术联合工程研究中心;
d.武汉市皮诺飞生物科技有限公司
ScienceDirect:《基于Ti3C2Tx MXene纳米片用于联合癌症治疗和抗炎的药物递送/级联酶系统》表明
摘要 高活性抗逆转录病毒疗法(highly active anti-retroviral therapy, HAART),又称鸡尾酒疗法,是治疗艾滋病最有前途的疗法之一。它包括三种或三种以上抗逆转录病毒药物的联合治疗,以较大限度地减少耐药性,较大限度地抑制病毒复制,且部分甚至完全恢复受损的免疫功能。因此,该疗法能有效延缓疾病的进程。同样,在癌症治疗领域,与单一疗法相比,两种或两种以上疗法的联合疗法因其治疗效果更好、副作用更少而备受关注。随着纳米医学的发展,目前的技术可以将各种治疗技术融入纳米粒子,通过增强渗透性和滞留(Enhance the permeability and retention, EPR)效应或主动靶向来实现肿瘤靶向治疗。通过纳米技术进行癌症综合治疗的方法多种多样,包括化疗、基因治疗、光疗、催化治疗、超声波治疗、免疫治疗等。其中,光疗因其无创、无损、无电离、简单、高效、低毒等特点而成为一种特别有用的方法,通常与其他疗法相结合,通过控制照射位置来精确治疗肿瘤。光动力疗法(PDT)通过光对光敏剂的照射产生活性氧(ROS)来消除靶细胞,或利用光照射具有高光热转换效率的材料来加热靶区,从而实现光热疗法(PTT)。将化疗与光热疗法结合使用可提高疗效。引入PTT可以提高依赖ROS的化学动力疗法(CDT)的疗效。特别是,与紫外-可见光(UV)相比,使用近红外(NIR)光作为光源更安全,且能更深地穿透组织。与光动力疗法相比,PTT更适合在缺氧环境中治疗实体瘤,因为它不需要氧气。此外,研究表明正常细胞比癌细胞更耐热,因此在PTT过程中可将对机体的损伤降至至低。总体而言,PTT更适合癌症精准治疗。不过,PTT也有一定的缺点,所需的高治疗温度仍会损伤正常细胞,另一个常见副作用是高热引起的坏死细胞膜破裂会释放细胞ROS,导致炎症。炎症是机体对组织损伤或病原体感染的一种自然而必要的反应,但它也在肿瘤发展的重要阶段(包括促进、侵袭和转移)发挥着关键作用。被称为MXenes的二维(2D)过渡金属碳化物、氮化物和碳氮化物是一类新型光热材料。自2017年以来,MXenes一直是热门研究课题,包括在生物医学领域。研究表明,MXenes不仅具有良好的生物相容性,其二维结构还可以负载药物、纳米颗粒等,制备过程中引入的官能团(如-OH)使其表面可以被改性。基于这些特性,MXenes在基于PTT的肿瘤联合治疗中得到了广泛应用。碳化钛(Ti3C2Tx)是2011年报道的MXene,它是通过蚀刻Ti3AlC2中的铝原子,然后用插层剂插层而成。它也是较早用于肿瘤PTT的MXenes。由于过渡金属的固有特性,Ti3C2Tx MXene中处于低价态的钛元素可被氧化剂(如ROS)氧化。这一特性赋予了Ti3C2Tx MXene可以在进行PTT治疗时清除ROS的能力,从而抑制炎症。我们课题组之前的研究表明,当Ti3C2Tx与具有抗炎特性的天然表没食子儿茶素没食子酸酯(Epigallocatechin gallate, EGCG)联合使用时,PTT在体外和体内引起的炎症均可完全消除。此外,第二章的研究内容已经证明,Ti3C2Tx还具有类似过氧化氢酶(CAT)的活性,能分解H2O2产生O2。这使得它有可能与其他依赖氧气的治疗方式相结合,包括基于葡萄糖氧化酶(GOx)的饥饿疗法和化疗,从而提高治疗效果。
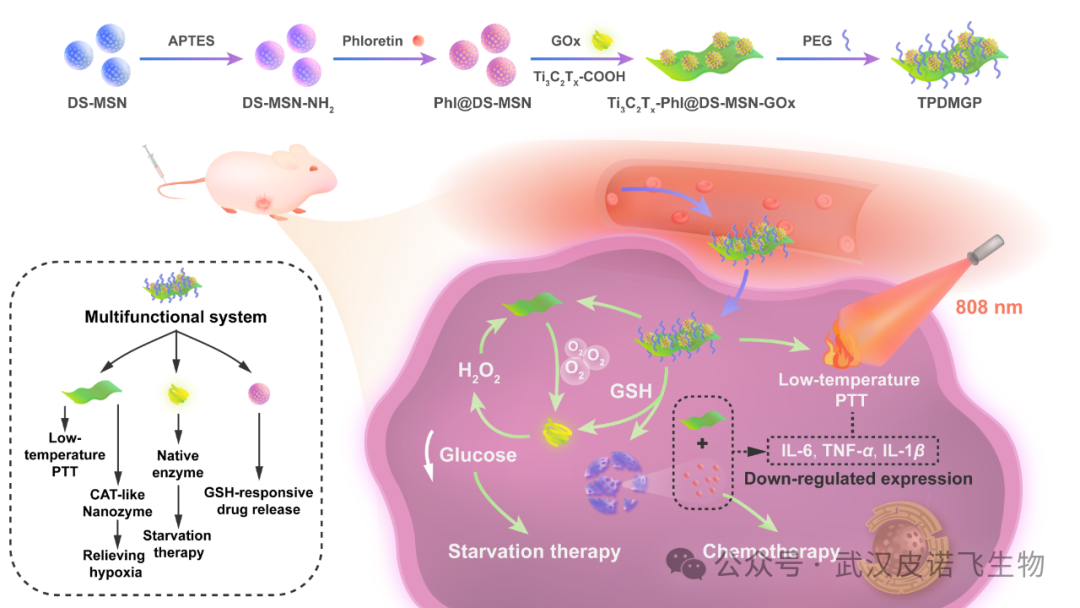
TPDMGP的制备过程及其增强联合治疗癌细胞的机制示意图
基于MXene的光热性能、抗炎特性以及类CAT活性,本章研究工作是,设计并构建了一种用于肿瘤联合治疗的纳米药物递送和级联酶系统,该系统能够消除治疗过程中产生的炎症反应。如图3.1所示,制备了骨架中含有氧化还原敏感二硫键的超小型可降解介孔二氧化硅纳米粒子(DS-MSN),用于负载根皮素(phloretin, Phl),将葡萄糖氧化酶(GOx)涂覆在得到的Phl@DS-MSN表面,然后沉积到Ti3C2Tx MXene纳米片上,再利用聚乙二醇(PEG)保护,得到的多功能抗肿瘤系统被命名为Ti3C2Tx-Phl@DS-MSN-GOx-PEG (TPDMGP)。Ti3C2Tx除了可用于PTT外,还能将癌细胞内的H2O2分解成O2,然后提供给GOx进行饥饿治疗。同时,GOx分解葡萄糖的产物之一H2O2可被Ti3C2Tx不断分解,循环提供O2。这样,一个酶级联系统就建立起来了,有助于改善饥饿疗法。癌细胞中高水平的谷胱甘肽(GSH)破坏DS-MSN骨架中的二硫键,导致其降解并释放出Phl。Phl是一种植物化合物,天然存在于苹果和梨等多汁水果的果皮和根皮中,具有抗氧化和抗炎特性,已被研究用作是治疗癌症的潜在化疗药物。然而,由于其溶解度较低,必须使用递送系统才能达到较高的血药浓度。因此,将其载入TPDMGP,可在癌细胞内控制释放。通过与Ti3C2Tx MXene联合给药,它可以有效的抑制癌细胞并消除PTT引起的炎症。通过与化疗/饥饿疗法相结合,TPDMGP的低温PTT可实现显著的肿瘤抑制,并有效抑制PTT引起的炎症。这项工作有望为拓展MXene在癌症治疗领域的应用提供创新思路。
